近日,中国科学院高能物理研究所多学科研究中心生物医学组与合作者在脂质纳米颗粒 (LNP)免疫识别机制研究方面取得重要进展,相关成果已发表于《美国化学会志》Journal of the American Chemical Society。研究团队开发了一种新方法,实现LNP与人体血液蛋白相互作用形成“蛋白冠”的原位动态分析,揭示LNP与免疫细胞受体之间的作用机制。
脂质纳米颗粒作为mRNA疫苗的核心递送系统,在体内循环过程中会快速吸附血浆蛋白形成动态"蛋白冠"。该蛋白冠的分子构成直接调控LNP的生物分布、靶向效率、免疫激活特性及代谢清除动力学。传统超速离心结合多步洗涤的分离方法因高剪切力可能导致LNP结构形变,同时多步洗涤造成蛋白冠组分解离,难以真实反映LNP-生物界面作用的机制。针对这一技术瓶颈,研究团队基于前期建立的蛋白冠动态分析方法(Nat. Commun. 2022, 13, 5389),开发了"原位垂钓"技术:通过化学键将LNP固定于生物传感器表面(图1),实现原位、无损监测蛋白冠形成的动态过程,并保持多层蛋白冠组分的完整性;进而结合原位解离策略与高灵敏质谱,成功解析了LNP蛋白冠的形成规律及其介导免疫细胞识别的膜受体。
据报道,经聚乙二醇(PEG)修饰的疫苗接种、PEG化纳米药物的重复给药以及环境暴露(如食品添加剂及日化用品中的PEG成分)均会显著提升人体内PEG特异性抗体的滴度,这种变化会重塑PEG化纳米载体的药代动力学行为。本研究通过 “原位垂钓”技术阐明了其机制,发现LNP表面形成的蛋白冠中选择性富集PEG抗体,进而促进免疫细胞通过集落刺激因子2受体β(CSF2RB)识别和清除LNP (图2)。这一发现解释了不同个体对PEG化纳米药物代谢速度的差异以及疫苗或纳米药物在多次使用后会被加速清除的机制。本研究不仅为设计更精准的mRNA疫苗和纳米药物提供了科学依据,也为优化纳米载体的免疫逃避策略提供了新思路。未来可尝试开发新型载体材料,如两性离子修饰、仿生结构或可降解纳米材料,以减少免疫系统对LNP的快速清除。
我所博士后Baimanov Didar、北京大学药学院王静副研究员为该论文共同第一作者,生物医学组王黎明研究员、国家纳米科学中心陈春英院士为通讯作者。上述工作得到了国家重点研发计划、国家自然科学基金、北京市自然科学基金、所创新项目、建制化科研平台等项目资助。
原文链接: https://pubs.acs.org/doi/10.1021/jacs.4c16987。
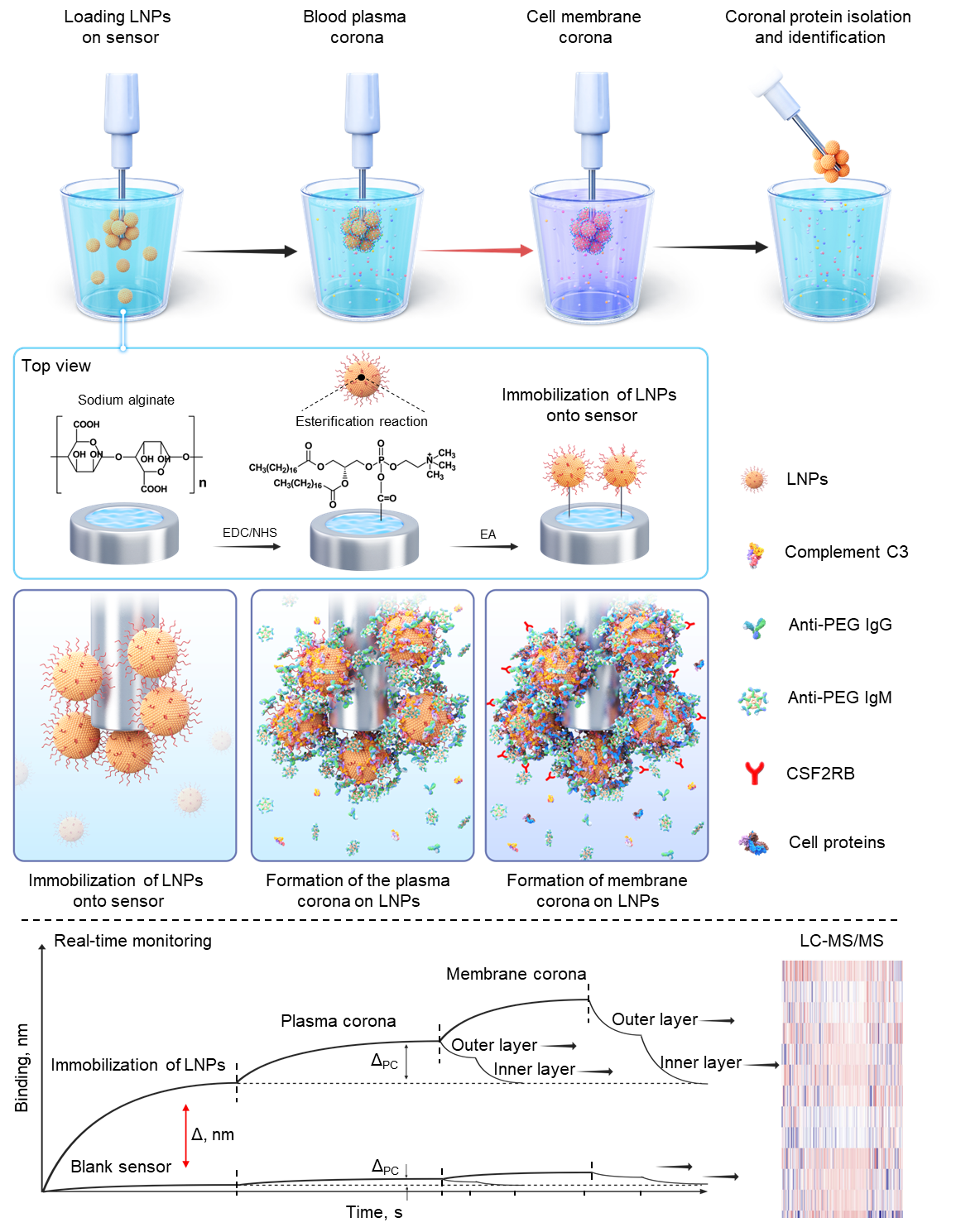
图1. 开发“原位垂钓”技术,用于鉴定LNP表面蛋白冠和细胞膜受体。
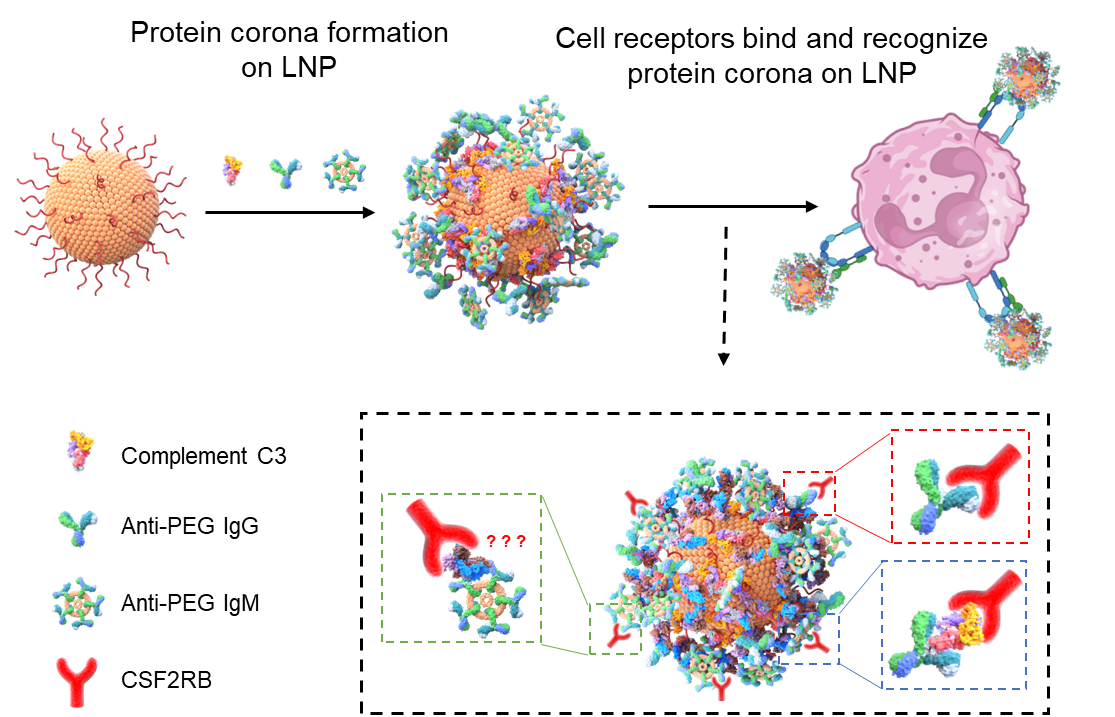
图2. LNP在血液中的行为受其血浆蛋白冠的影响,并通过PEG抗体与补体等途径与髓系细胞受体识别,介导LNP胞吞。
附件下载: